1.設立の背景と主旨
本ワーキンググループは、本邦の乳癌診療や研究におけるビッグデータ医療/研究(人工知能や統計学、科学的手法、データ分析など)の目指すべき方向性やそのために必要な人・モノ・資金を確保するための方策について検討していくことを目的として設立された。
具体的には、国内の乳癌領域におけるReal-World Evidence(RWE)を集積するネットワークを構築し、国際的に通用するデータベースを設立・維持して研究を進めることで、日本の乳癌研究をさらに発展させることを目指している。
2.メンバー構成と役割分担
座長として佐治重衡(福島県立医科大学 腫瘍内科学講座)と森田智視(京都大学大学院医学研究科 医学統計生物情報学)の両名がつとめ、委員として高野利実(がん研究会有明病院 乳腺内科)、相良安昭(相良病院)、増田紘子(昭和大学医学部 乳腺外科)、そして外部委員として黒田知宏(京都大学医学部附属病院 医療情報企画部)が就任した。各自の専門性を最大活用し、協働して検討にあたることになった。(敬称略)
- 臨床的側面からビッグデータにより達成すべきゴール(研究成果)の検討:佐治、高野、相良、増田
- ビッグデータの管理・保管や分析方法の検討データ分析:森田、相良
- 医療情報システム・管理・活用の立場からの助言:黒田
活動内容:
2023年5月15日 第1回会議
2023年8月21日 有識者会議 1
講師:中村 理彦 先生(IQVIA Japan Group Real-World & Analytics Solutions)
内容:OMOPなどのデータマッピングを用いて、異なる電子カルテから国際標準規格のデータベースを構築する方法や、症例情報を施設外に出さずに解析結果のみを統合するデータ構築についてのご講演をいただいた。
2023年12月21日 有識者会議 2
講師:黒田知宏 先生(京都大学医学部附属病院 医療情報企画部 教授)
内容:電子カルテを主軸にしたデータ構築や人によるデータ入力に頼らないデータ集積システム構築、医療AIの利用など、次世代の医療情報基盤を構築するための新たな展開についてのご講演をいただいた。また、フィンランドの医療二次データ利用制度を引用し、医療データのより積極的な活用のためには法的な整備についてさらに議論を重ねていくことの重要性を強調されていた。
その他にNCD(National Clinical Database)、IQVIA 、JBCS事務局、WGメンバー、登録データサイエンス委員会委員などを交えた会議を複数回実施した。
3.アプローチの仕方と方法
Real-World Data(RWD)からRWEを効率的、効果的に創出するためには、段階を追って課題がある。1つ目は構造化、2つ目は個人情報保護、3つ目は標準化・正規化である。
電子カルテシステムや病院情報システムに由来するRWDには検査結果、画像、判断根拠など重要なアウトカム情報が含まれる。一方で、これらは非構造情報であり、統計解析を試みるためにはデータの構造化処理が必須となり、RWD活用におけるハードルとなっている。一方、レジストリ研究に代表されるように、入力段階で構造化テーブルを作成することも一案であるが、この場合にも結局は入力時に労力を要することとなる点においては変わりがない。
個人情報保護もまたRWD利活用における重要な視点である。RWDは個人識別符号または要配慮個人情報を含むケースがほとんどである。データによっては、遺伝子配列情報など、そもそも匿名化自体が成立しないものがあり、また再特定リスクを下げるべく加工を入念に行った結果、データの価値そのものを棄損してしまうことも少なくない。
さらに、データの標準化・正規化も大きな課題である。“ビッグデータ解析“の観点から、異なるデータセットを比較・統合することはRWEの創出において極めて有効な手法であるが、そのためにはデータセット間の規格が統一されている必要がある。特に、RWDの利活用の幅を狭めないためには、国内に限定されるようなガラパゴス規格ではなく、国際的な標準規格の採用を念頭に置くことが重要である。
本ワーキンググループでは、上記の課題解決の方法として、AI(自然言語処理技術)とRWD Common Data Model(CDM)の採用を検討している。自然言語処理技術により、既存テキスト情報を構造化処理することで入力に要する労力の削減が可能となる。またRWD CDMの採用は、データ解析の前処理に係る労力を削減できるだけでなく、同じRWD CDMを採用している他のデータセットとの比較・統合解析を用意にすることができる。
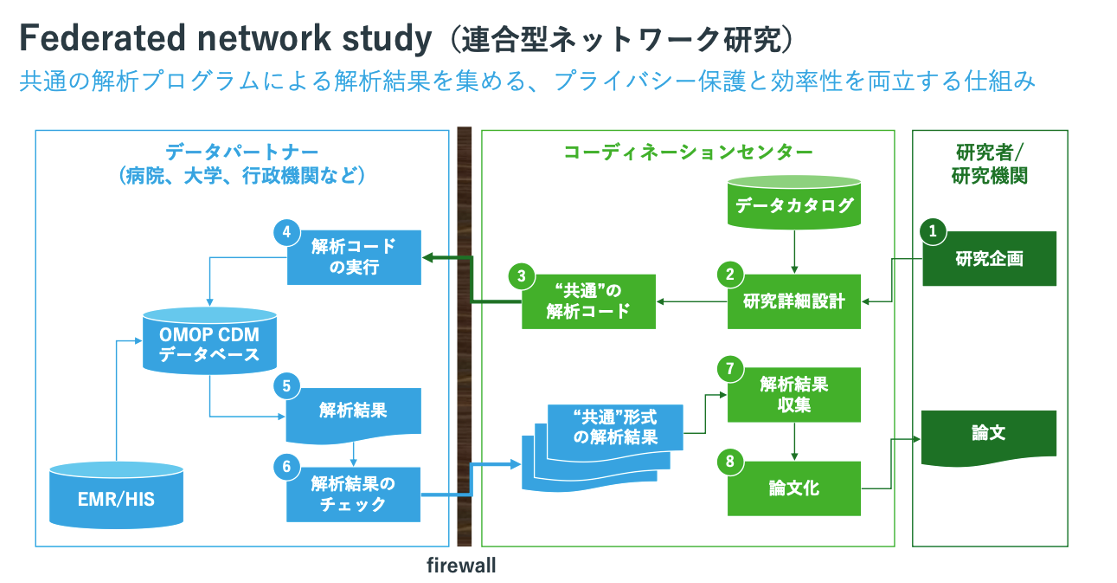
RWD CDMとしては、解析目的に強みをもつOMOP CDM(Observational Medical Outcomes Partnership Common Data Model)の採用を検討している。国内乳癌治療施設においてそれぞれ異なる電子カルテシステム等の臨床情報からOMOP CDMに統一することで、症例情報を施設外に出さずに解析結果を統合する連合型ネットワークの体制構築を検討している(下図)。連合型の形式は、上記課題のうち個人情報保護に対する解決策として、欧州を始めとする諸外国において導入が進められている。
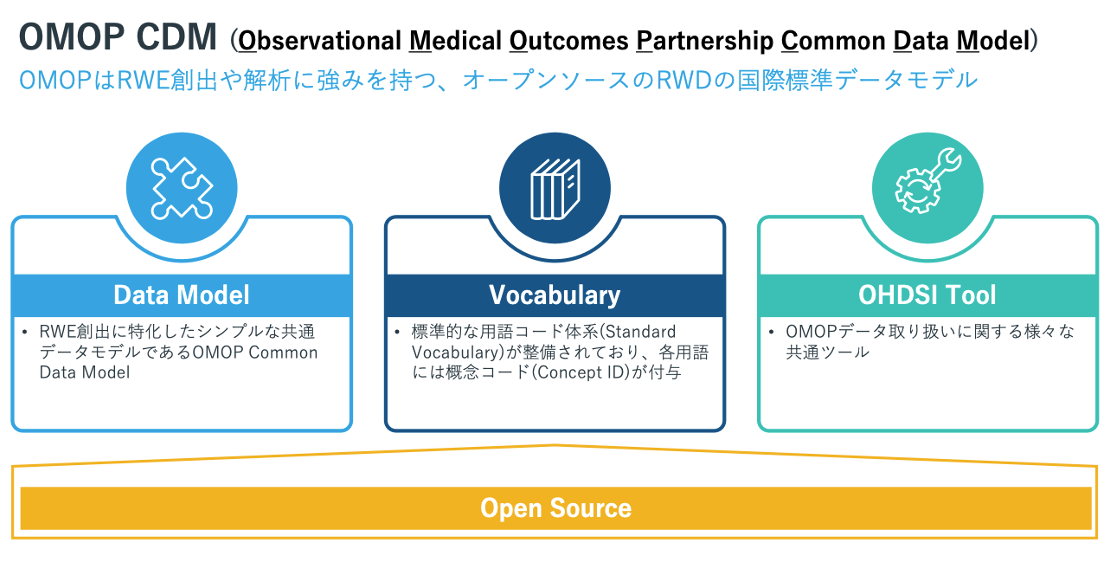
OMOP CDMは、異なる形式や構造の医療データ(電子カルテ、保険請求データ、臨床試験データなど)を一貫した形式に変換し、さまざまな研究や解析に利用できる1。OMOP CDMは(下図)にも示すように、主に以下の特徴を持っている。
- データの標準化:データ形式や用語を統一することで、異なるデータソース間での互換性を確保する。
- 大規模データ解析:大規模な医療データの解析が可能であり、特に疫学研究や薬剤の安全性評価に利用される。
- オープンソース:OMOPはオープンソースであり、世界中の研究者が利活用し、コミュニティによって常に進化している。
- 研究ネットワーク:OMOPは、Observational Health Data Sciences and Informatics(OHDSI)という国際的なオープンサイエンスコミュニティにより維持・管理されており、OHDSIネットワークを通じて様々な医療研究が行われている。
今後は日本乳癌学会データサイエンス委員会において、日本乳癌学会、国内の医療機関および研究機関、IQVIA、その他の企業と一緒に協働し、OMOP CDMを用いた国内の乳癌データベース構築を以下のフェーズに沿って取り組んでいく予定である。
- フェーズ1:コンソーシアムの形成とデータセットの定義、システム調査と要件定義。NCD(National Clinical Database)への症例アップロード機能付加の検討。
- フェーズ2:Proof of Concept(PoC)として、国内5つの施設でパイロット研究開始。各施設にてデータベースを構築し、OMOP CDMへの変換を実施。PoC参加施設における連合解析研究の実施。
- フェーズ3:日本乳癌学会に参加している施設への展開。国内の多施設データを使用した大規模研究の企画と実施。国内外DBを使った大規模研究の企画と実施。
4.採用した手法の根拠と妥当性
OMOPは、臨床情報の解析とRWEの創出に特化した国際標準のデータモデルであり、多くの国際的なプロジェクトで採用されている2,3。
各施設の電子カルテ等の情報をOMOP CDMを用いてデータマッピングを行い、院内データベースが構築されることにより、医師やデータマネージャの手作業による症例情報の入力が不要となり、各施設の電子カルテ等の情報から自動的にデータベースが構築されることになる。各施設はそのデータベースから、NCDへの症例登録も可能となり人件費の削減にもつながる。データは原則として院内環境下に運用して頂き、研究目的などに応じて院外にデータ提供が必要な場合には別途適切なプロセスをとる。
このデータベースは施設間でネットワーク化することが可能となり、症例データや個人情報を院外に出さない形で解析が可能となる。従って、多施設の医療情報の解析や研究を行うために患者同意が不要であり、国内のRWE創出に大きな貢献をもたらすことが期待される。
5.成果、結果、解釈
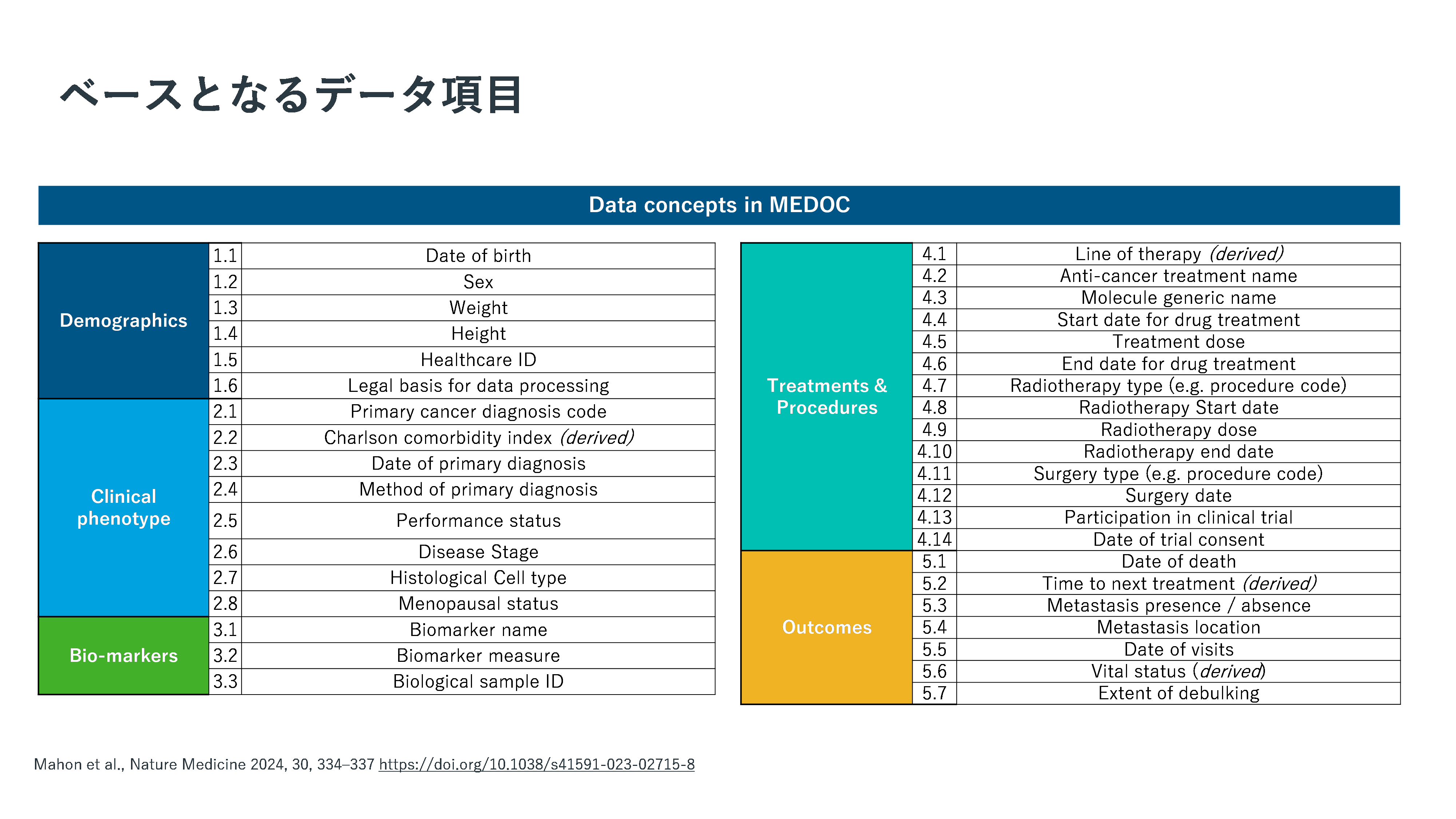
まず、国内5つの施設においてPoCが実施される予定である。今回は、OMOPの中で先行研究実績のあるDigiONE(the DIGItal Oncology Network for Europe)の乳癌研究用項目(DIGIONE03)3をベースとすることで(下図)、データ構築のフィージビリティを担保しながら将来的な国際研究に対する基盤を整備していく予定である。
自施設/参加施設のOMOPデータの学術研究目的への利用やNCD登録データの目的内利用が可能とし、各施設におけるデータ抽出ツールの利用ができるようになる予定である。連合型ネットワーク研究の成果として、データの標準化と統合データの解析結果の公表を行う。
6.限界と課題
以下の課題が挙げられるが、今後のプロジェクト進行において解決していく必要がある。
- データの標準化における技術的なハードル
- 医療データの二次利用に関するハードル
- 各施設や企業、学会間でのデータの取り扱いや資金に関して、透明性の高い仕組みの構築
- データ構築ならびに活用の対価に見合う公正市場価値の設定
- 各団体における法務部門で各団体間での上記契約案を作成
- RWEネットワークを持続的に運用していくためのエコシステムの構築
7.将来展望
日本乳癌学会や学会認定施設、大学、企業などが協働したコンソーシアムを形成し、拡大・継続していくことを想定している。国際的なDigiONEプロジェクトとの比較・統合研究が可能となる基盤を整備する。また、医療AI技術の進展を的確に把握しその積極的な活用をすすめることで国際水準のデータベース構築を目指す。
<参考文献>
- Hallinan CM, Ward R, Hart GK, et al. Seamless EMR data access: Integrated governance, digital health and the OMOP-CDM. BMJ Heal care informatics. 2024;31(1). doi:10.1136/bmjhci-2023-100953
- Omar MI, Roobol MJ, Ribal MJ, et al. Introducing PIONEER: a project to harness big data in prostate cancer research. Nat Rev Urol. 2020;17(6):351-361. doi:10.1038/s41585-020-0324-x
- Mahon P, Chatzitheofilou I, Dekker A, et al. A federated learning system for precision oncology in Europe: DigiONE. Nat Med. 2024;30(2):334-337. doi:10.1038/s41591-023-02715-8
AI-ワーキンググループ
ビッグデータサイエンス ワーキンググループ
リスク評価ワーキンググループ
リキッドバイオプシーワーキンググループ
乳腺ロボット手術ワーキンググループ
乳癌ラジオ波焼灼療法検討ワーキング
乳房再建に関するワーキンググループ(2022年-2024年)
大学教育に関するワーキンググループ